DEMANDA BIOQUíMICA DE OXíGENO
(DBO5).
DETERMINACION MEDIANTE
EL USO DE BOTELLAS RESPIROMETRICAS.
EFECTO DE LA CONCENTRACION DEL BUFFER DE FOSFATO SOBRE EL pH Y EL RESULTADO
DEL PROCESO.
Por:
Felipe Calderón Sáenz y Margarita Pavlova.
Dr. Calderón Laboratorios Ltda.
Abril 29 de 2001
www.drcalderonlabs.com
Avda. 13 No. 87-81
Bogotá D.C., Colombia S.A.
acaldero@cable.net.co
INTRODUCCION
Se presentan en el siguiente reporte los resultados de la investigación realizada con Botellas respirométricas para determinar el efecto de la concentración de la solución tampón de fosfato sobre el pH inicial y final de la solución, la captación de CO2 y la lectura de la depresión final en las botellas.
Durante la determinación respirométrica de la DBO5 se libera CO2 en la solución, el cual debe ser captado para poder medir el consumo de oxígeno en base a la depresión en el interior de las botellas. Uno de los métodos propuestos (1), consiste en agregar a la solución una cantidad adecuada de solución tampón de Fosfato Disódico y Fosfato Dipotásico, los cuales tienen la misión de captar el CO2 transformándolo en bicarbonato de Sodio y Potasio respectivamente. A medida que avanza el proceso, la producción de CO2 (ácido carbónico) causa una reducción del pH del medio. Esta reducción del pH, de llegar a ser muy pronunciada, impediría la captación adecuada del CO2 y por consiguiente alteraría los resultados.
Por otro lado, el pH óptimo para el desarrollo de las bacterias está comprendido entre la neutralidad y ligeramente alcalino (2), (3).
Con el fin de comprobar el efecto de esta variación se realizó un experimento con diversas dosificaciones de Solución tampón de fosfato y se midió su efecto sobre el resultado final del pH así como sobre el resultado de la determinación de la DBO5.
Se utilizaron 12 botellas con volúmen de 525 ml c/u y un patrón de Glucosa-Acido Glutámico (GGA) 50X. Como inóculo se utilizó agua del caño.
MATERIALES Y METODOS
Se monto un experimentto con cuatro tratamientos y tres replicaciones consistente en un total de 12 Botellas respirométricas de 525 ml c/u, distribuidas como aparece en la siguiente tabla:
|
No. de la Botella
|
Tratamiento
|
Solución Tampón de Fosfato
|
|
1
|
Serie 1
|
2 ml
|
|
2
|
-- " --
|
2 ml
|
|
3
|
-- " --
|
2 ml
|
|
4
|
Serie 2
|
3 ml
|
|
5
|
-- " --
|
3 ml
|
|
6
|
-- " --
|
3 ml
|
|
7
|
Serie 3
|
4 ml
|
|
8
|
-- " --
|
4 ml
|
|
9
|
-- " --
|
4 ml
|
|
10
|
Serie 4
|
5 ml
|
|
11
|
-- " --
|
5 ml
|
|
12
|
-- " --
|
5 ml
|
La Botellas se cargaron con los siguientes reactivos: (Ver Preparación de Reactivos en: Metodo Respirometrico....)
a.- 4 ml de Solución de Glucosa Acido Glutámico (GGA) 50X
b.- Solución Tampón de Fosfato (2X); tal como se indica en la
tabla anterior.
c.- 0.25 ml de Solución B (Sulfato de Magnesio)
d.- 0.25 ml de Solución C (Cloruro de Calcio)
e.- 1 gota de Solución D (Cloruro Férrico 10X)
f.- 4 gotas de Agua de Inóculo (Agua de Caño)
Acto seguido se aforaron a 250 ml con Agua destilada y se colocaron en las Botellas de 525 ml.
Se colocarón las Botellas en la Incubadora, a 20 °C ±1°
y se inició el programa de agitación intermitente. Se tomó
una lectura de la depresión interna de las botellas al principio del
experimento y luego una lectura cada 24 horas durante 7 días.
RESULTADOS
Con las lecturas de la depresión de las botellas se calculó el consumo de oxígeno mediante el programa Calculos DBO5 y se expresó el resultado en mg/lt referidos a la alícuota inicial del Patrón 50X.
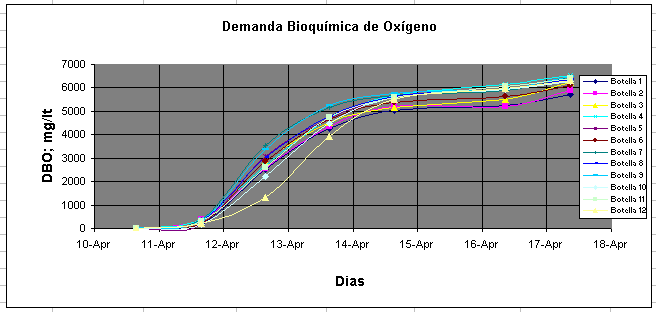
Los resultados de todas las leccturas realizadas pueden verse en el gráfico siguiente en el cual se han calculado los resultados de la DBO5 para el Patrón de Glucosa-Acido Glutámico (50X).

Las diferencias entre tratamientos fueron pequeñas pero altamente significativas. El menor resultado se obtuvo con la menor concentración de la solución buffer. En el gráfico siguiente pueden apreciarse los promedios de DBO5 para cada uno de los tratamientos siendo la "Serie 1" la de menor concentración de la solución buffer.

El resultado del pH puede verse en la gráfica siguiente:

A medida que se incrementó la dosis de Buffer, se observó un aumento tanto en el pH inicial como en el pH final en forma lineal y altamente significativa. El pH inicial estuvo comprendido entre 7.68 y 7.73 para la menor dosis de Buffer y entre 8.06 8.13 para las dosis mas altas del buffer. Este rango de pH se considera favorable para el desarrollo de las bacterias. El pH final estuvo entre 6.77 y 6.81 para la menor dosis del buffer y entre 7.23 y 7.33 para la mayor dosis del buffer.
A un pH Final por debajo de 6.9 se obtuvieron valores de DBO5 significativamente menores que a mayores valores de pH.
DISCUSION
Con relación al pH Final es de notar que la menor dosis de Buffer afecto significativamente la medición de DBO5. Este resultado podría deberse a dos causas. a) Falta de captación del CO2 por parte del medio y b) Menor trabajo de las bacterias y por ende menor consumo de oxígeno. Este efecto puede verse en la gráfica siguiente.

Aplicando el diagrama de Cate y Nelson, podríamos decir que el pH crítico para la determinación es de 6.9
CONCLUSIONES
Los resultados de este experimento permiten obtener, entre otras, las siguientes conclusiones:
1. Las mejores dosis para la concentración de la solución Buffer
de Fosfato que mejor responden desde el punto de vista de captación del
CO2 tanto como para obtener el pH mas adecuado al trabajo de las bacterias fueron
las de 4 y 5 ml de solución Buffer (2X).
2. El Consumo de Oxígeno en este experimento fue casi idéntico
al de otros experimentos realizados bajo condiciones de agitación intermitente.
3. El pH original del agua así como su capacidad tampón afectan
el resultado y obligan a ajustar el pH de la misma antes de iniciar la prueba.
4. De acuerdo con los resultados de este trabajo, un pH inicial para el proceso
de 8.2, aparentemente no afecta el trabajo de las bacterias y posiblemente al
cabo del segundo día ya el pH haya bajado a menos de 7.5
RECOMENDACIONES
1. Realizar pruebas de reconocimiento con la solución Tampón
de Fosfato (2X) con aguas residuales de diferentes pHs originales.
2. Realizar una prueba con agitación intermitente y colocando las botellas
en posición cuasi-horizontal con el fin de facilitar el intercambio gaseoso
entre la atmósfera interior de la botella y el líquido.
BIBLIOGRAFIA
1.Dterminación de la Demanda Bioquímica de Oxígeno DBO5;
Método Respirométrico; Calderón Sáenz, Felipe; Pavlova,
Margarita; Bogotá, Enero 15 de 2001; Rev. Enero31/2001; www.drcalderonlabs.com
2.Investigación sobre el uso de Botellas Respirométricas para
la determinación de la Demanda BioQuímica de Oxígeno;
3. Microorganisnos y su Fertilidad. Prof Dr. Vacile Rankov, Gizda Ampova et.
al. Ed. Zemisdad, Sofia, 1983
4. Introducción a la Microbiología del Suelo. Martin Alexander.
Ed AGT Editorial S.A., Mexico, 1980
FIN
Dr. Calderon Labs.